2025年10月,北京师范大学心理学部认知神经科学与学习国家重点实验室舒妮教授及合作者在《Genome Medicine》(IF:11.2)发表题为“Polygenic risk for Alzheimer’s disease in healthy aging: age-related and APOE-driven effects on brain structures and cognition”的研究论文。该研究基于英国生物银行(UK Biobank)2万余名健康老龄个体的影像遗传学数据,系统解析了阿尔茨海默病多基因风险与脑结构和认知衰退的年龄依赖关系,揭示了高遗传风险人群在认知老化过程中海马-丘脑系统结构加速退化并导致认知下降的神经机制,为老年脑健康风险评估和早期干预提供了重要参考。
阿尔茨海默病(Alzheimer’s disease, AD)是老年期最常见的神经退行性疾病,其遗传风险由数百个基因共同塑造,其中载脂蛋白E(APOE)ε4等位基因是散发性AD最强的遗传风险因素。研究团队利用约数百万个全基因组变异构建了AD多基因风险评分(AD-PRS),在控制性别、教育、疾病史及40个遗传主成分的条件下,系统分析了自然老化过程中AD多基因风险对脑结构和认知功能的影响。
相比于低遗传风险个体,高AD-PRS个体在海马、丘脑和内侧颞叶灰质体积随老化加速萎缩(图1),并表现出脑室扩大和白质完整性受损(尤其在穹隆与扣带回,图2);这些结构改变呈显著年龄放大效应:约自55岁起出现差异,在75岁后最为明显。此外,高AD遗传风险者在执行功能、记忆和推理功能上随老化加速衰退,这一趋势主要通过海马-丘脑及其白质纤维连接的结构退化所中介(图3)。进一步敏感性分析表明,APOE基因在AD遗传风险中具有主导作用,但非APOE多基因变异也对白质微结构完整性和执行功能有一定影响。这些非APOE遗传风险同时与脑血管及免疫通路相关,提示AD与心脑血管疾病在遗传层面存在潜在交叉。
本研究结合大样本基因-影像数据集,实现了连续年龄段上遗传效应的时空追踪,揭示了AD遗传风险在健康老龄化群体中的动态演化过程。研究成果阐明 AD 多基因遗传风险对脑结构与认知功能在自然老化进程中的效应轨迹,为老年期认知衰退的早期预测与干预提供了科学依据:对于高遗传风险人群,60岁前即可进行脑结构监测,并结合生活方式及环境因素制定个性化防控策略。
论文第一作者为北师大已毕业的陈豪杰博士(现为香港科技大学生命科学部博士后),通讯作者为北师大舒妮教授与中日友好医院马国林教授。合作单位包括北京师范大学、中日友好医院、首都医科大学宣武医院、南京航空航天大学等多个机构。该研究得到了国家科技创新2030-“脑科学与类脑研究”重大项目、国家自然科学基金及北京市自然科学基金等项目资助。
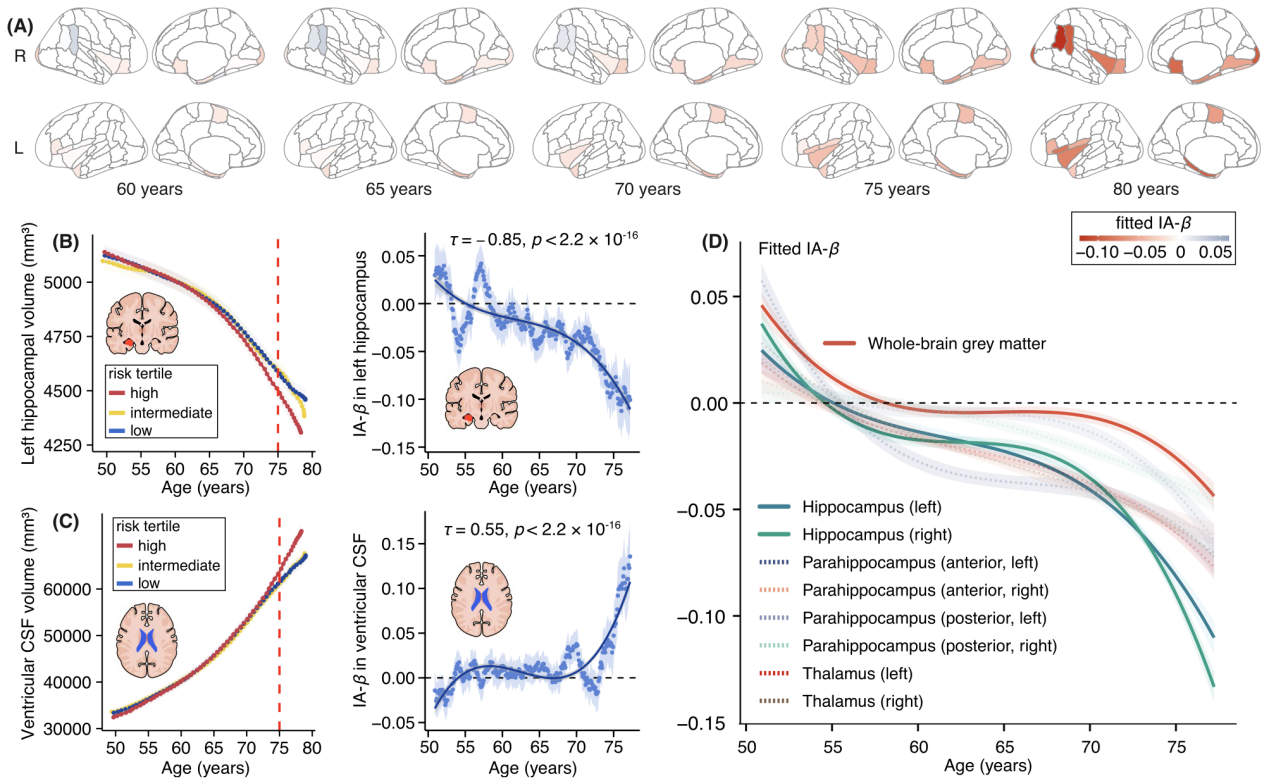
图1 AD-PRS对脑灰质体积的随龄效应轨迹
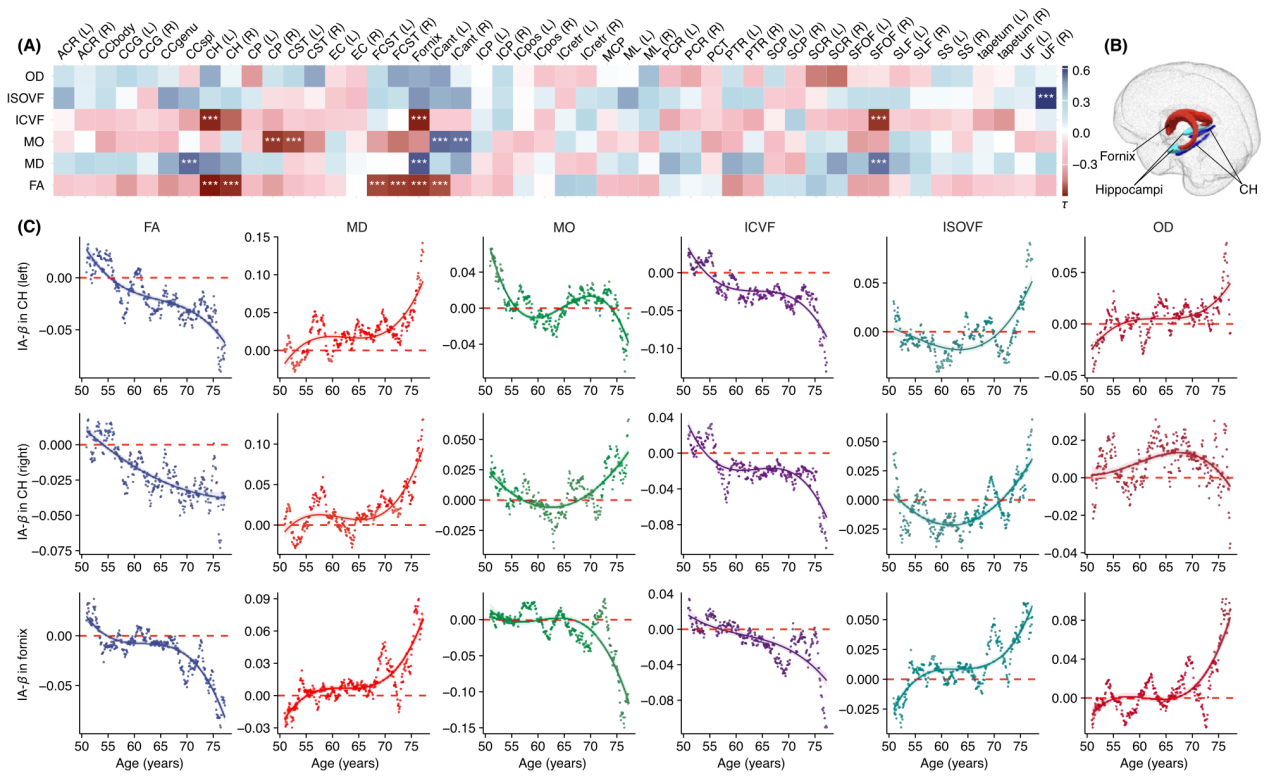
图2 AD-PRS对白质纤维束完整性的随龄效应轨迹
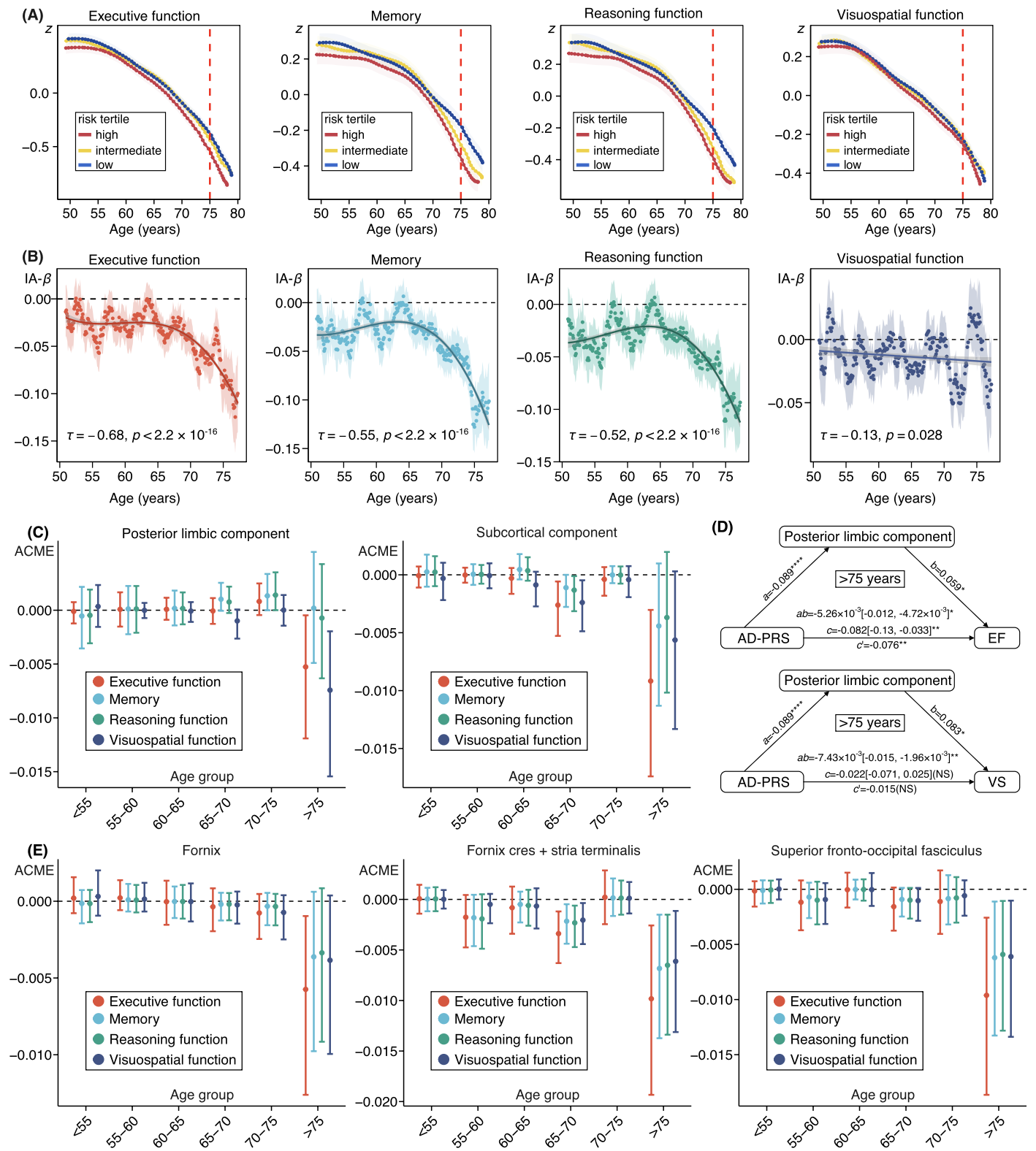
图3 受年龄影响的“基因-脑-认知”关联模型
论文链接:
https://genomemedicine.biomedcentral.com/articles/10.1186/s13073-025-01548-z